(S)-izoserinë 15a (21 g, 0,20 mol) u tret në tetrahidrofuran (100 mL) dhe u shpërnda një tretës i përzier me 10 për qind tretësirë ujore të hidroksidit të natriumit (100 mL), dikarbonat di-tert-butil (50 mL, 0,22 mol) Reaksioni u krye në temperaturën e dhomës për 9 orë. Faza ujore u rregullua në pH 2 me acid klorhidrik 4 mol/L dhe u nxor me diklorometan/metanol (v/v = 5/1, 50 mL × 3 ) dhe thahen mbi sulfat natriumi anhidrik. Filtro me thithje, koncentrat nën presion të reduktuar, Përbërja e titullit 15b u përftua si vaj pa ngjyrë (35 g, rendimenti: 85 përqind).
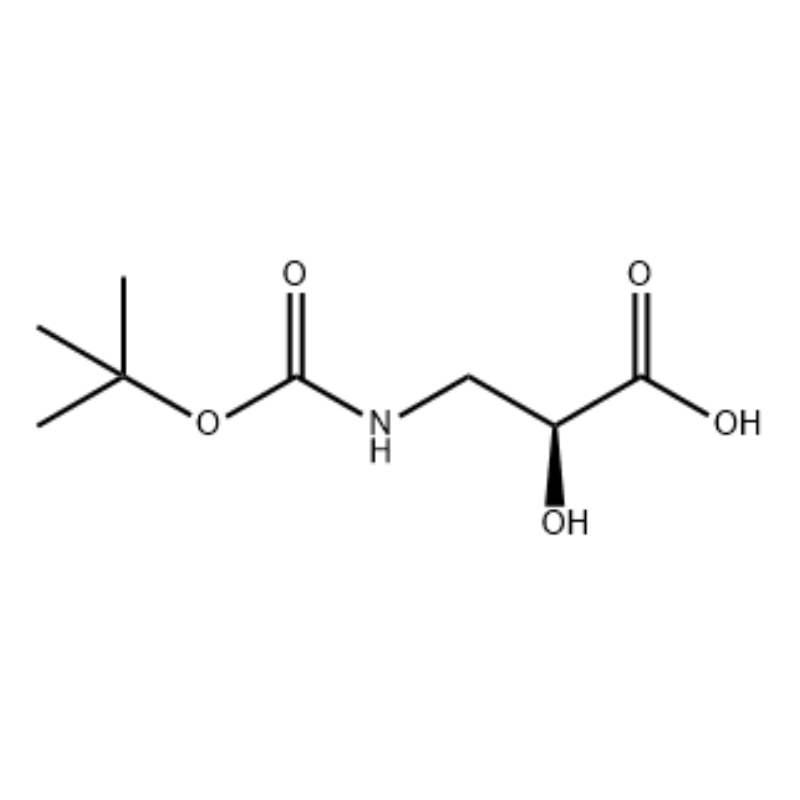
Në një tretësirë nxitëse të S-izoserinës (4.0 g, 0.038 mol) në dioksan: H2O (100 mL, 1:1 v/v) në 0°C iu shtua N-metilmorfolinë (4.77 mL, 0.043 mol), e ndjekur nga BoC2O (11.28 mL, 0.049 mol) dhe reagimi u trazua gjatë natës me ngrohje graduale në temperaturën e dhomës.Më pas u shtua glicinë (1.0 g, 0.013 mol) dhe reaksioni u trazua për 20 min.Reaksioni u fto në O0C dhe u ul aq.U shtua NaHCO3 (75 mL).Shtresa ujore u la me acetat etilik (2 x 60 mL) dhe më pas u acidifikua në pH 1 me NaHSO4.Kjo tretësirë u nxor më pas me acetat etilik (3 x 70 mL) dhe këto shtresa organike të kombinuara u thanë mbi Na2SO4, u filtruan dhe u përqendruan deri në tharje për të dhënë acidin e dëshiruar N-Boc-3-ammo-2(S)-hidroksi-propanoik. (6,30 g, 0,031 mmol, rendimenti 81,5 përqind): 1H NMR (400 MHz, CDC13) δ 7,45 (bs, 1 H), 5,28 (bs, 1 H), 4,26 (m, 1 H), 3,40-3,62 (m , 2 H), 2,09 (s, 1 H), 1,42 (s, 9 H);13C NMR (IOO MHz, CDC13) δ 174,72, 158,17, 82, 71,85, 44,28, 28,45.
acid N-Boc-3-amino-2(S)-hidroksi-propionik;Në një tretësirë nxitëse të S-izoserinës (4.0 g, 0.038 mol) në dioksan: H2O (100 mL, 1:1 v/v) në 0°C iu shtua N-metilmorfolinë (4.77 mL, 0.043 mol), e ndjekur nga BoC2O (11.28 mL, 0.049 mol) dhe reagimi u trazua gjatë natës me ngrohje graduale në temperaturën e dhomës.Më pas u shtua glicinë (1.0 g, 0.013 mol) dhe reaksioni u trazua për 20 min.Reaksioni u fto në 0°C dhe u ul në ujë.U shtua NaHCO3 (75 mL).Shtresa ujore u la me acetat etilik (2 x 60 mL) dhe më pas u acidifikua në pH 1 me NaHSO4.Kjo tretësirë u nxor më pas me acetat etilik (3 x 70 mL) dhe këto shtresa organike të kombinuara u thanë mbi Na2SO4, u filtruan dhe u përqendruan deri në tharje për të dhënë acidin e dëshiruar N-Boc-3-amino-2(5)-hidroksi-propanoik. (6,30 g, 0,031 mmol, rendimenti 81,5 përqind): 1H NMR (400 MHz, CDC13) δ 7,45 (bs, 1 H), 5,28 (bs, 1 H), 4,26 (m, 1 H), 3,40-3,62 (m , 2 H), 2,09 (s, 1 H), 1,42 (s, 9 H);13C NMR (100 MHz, CDC13) δ 174,72, 158,17, 82, 71,85, 44,28, 28,45.
 Ndërtesa 12, Nr.309, Rruga e 2-të Jugore, Zona e Zhvillimit Ekonomik, Distrikti Longquanyi, Chengdu, Sichuan, Kinë.
Ndërtesa 12, Nr.309, Rruga e 2-të Jugore, Zona e Zhvillimit Ekonomik, Distrikti Longquanyi, Chengdu, Sichuan, Kinë. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404

















.png)


