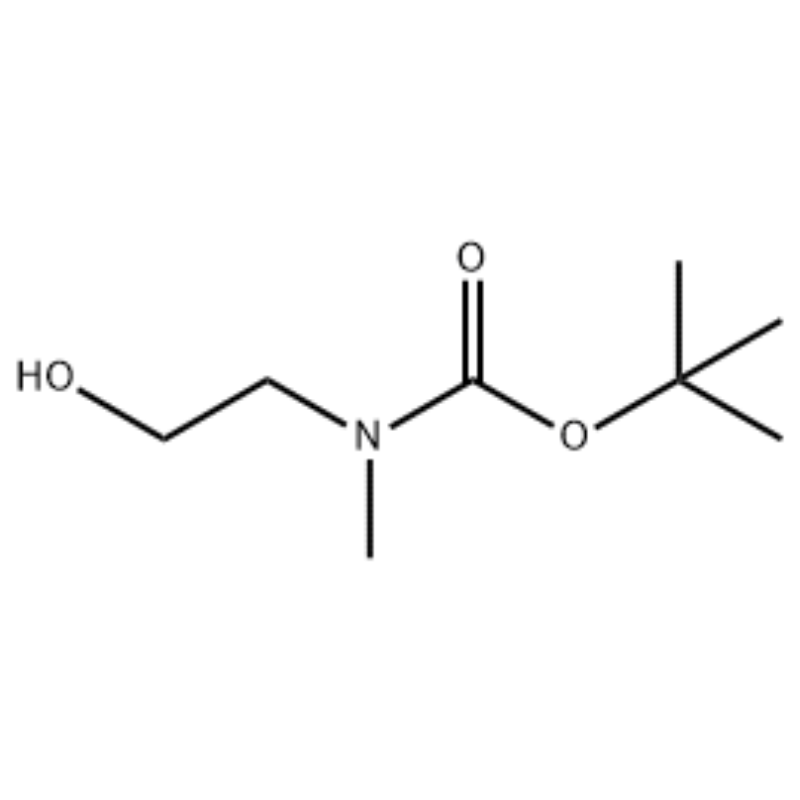
Në një tretësirë të 2-(metilamino)etanolit (500 mg, 0.53 ml, 6.66 mmol) në CH2Cl2 (20 ml) u shtua Boc2O (1.48 g, 6.79 mmol), e ndjekur nga përzierja në temperaturën e dhomës për 1 orë.Tretësira e reaksionit u ekstraktua me shëllirë dhe CH2Cl2.Shtresa organike e përftuar në këtë mënyrë u tha mbi MgSO4 dhe u filtrua.Më pas, filtrati u përqendrua në vakuo për të marrë përbërjen objekt (vaj pa ngjyrë, sasior);1H NMR (200 MHz, CDCl3) delta 3.74 (q, J= 10.5, 5.2 Hz, 2H) 3.25 (t, J= 5.2 Hz, 2H) 2.91 (s, 3H) 1.45 (s, 9H);spektri masiv m/e (intensiteti relativ) 144 (20) 102 (24) 57 (70) 44 (100).
Shembulli 38;N1-(3-Fluoro-4-(2-(1-(2-(metilamino)etil)-1H-imidazol-4-il)tieno[3,2-b]piridin-7-iloksi)fenil)-N3 -(2-metoksifenil)malonamide (96);Hapi 1: tert-Butil 2-hidroksietil(metil)karbamat (97) (J. Med. Chem., 1999, 42, 11, 2008) Në një tretësirë të 2-(metilamino)etanolit (5.0 g, 67 mmol) në THF (50 ml) në RT u shtua Boc2O (15.7 g, 72 mmol) dhe përzierja e reaksionit u trazua në RT për 4 orë.Përzierja e reaksionit u përqendrua deri në tharje dhe komponimi i titullit 97 u përdor drejtpërdrejt në hapin tjetër pa pastrim shtesë (11.74 g, rendiment 100%).MS (m/z): 176.2 (M+H).
Përgatitja e l-2-[4-Bromo-2-(4-okso-2-ftiotaiokso1hiazolidin-5-ilidenemefliil)fenoksi]efliil-3-efliil-l-metilurea(Compoiotamd 161)Hapi 1: Sinteza e t-butil hidroksietilmetilkarbamat;Në një tretësirë të 2-(metilamino)etanolit (500 mg, 0.53 ml, 6.66 mmol) në CH2Cl2 (20 ml) u shtua BoC2O (1.48 g, 6.79 mmol), e ndjekur nga përzierja në temperaturën e dhomës për 1 orë.Tretësira e reaksionit u ekstraktua me shëllirë dhe CH2Cl2.Shtresa organike e përftuar në këtë mënyrë u tha mbi MgSO4 dhe u filtrua.Më pas, filtrati u përqendrua në vakuo për të marrë përbërjen objekt (vaj pa ngjyrë, sasiore);1HNMR (200 MHz, CDCl3) delta 3.74 (q, J= 10.5, 5.2 Hz, 2H) 3.25 (t, J= 5.2 Hz, 2H) 2.91 (s, 3H) 1.45 (s, 9H);spektri masiv m/e (intensiteti relativ) 144 (20) 102 (24) 57 (70) 44 (100).
2-(metilamino)etanol (90.1 g, 1.2 mol) u tret në 1.2 L klorur metilen dhe BoC2O (218 g, 1 mol) u shtua ngadalë në të duke u trazuar në 00C, e ndjekur nga në temperaturën e dhomës për 3 orë.Përzierja e reaksionit u la në mënyrë sekuenciale me 700 mL të një tretësire ujore të klorurit të amonit të ngopur dhe 300 mL ujë.Përzierja e larë u dehidratua duke përdorur sulfat natriumi anhidrik dhe u përqendrua nën një presion të reduktuar, për të marrë përbërjen (a) (175 g, 1 mol, 100%) si një vaj pa ngjyrë. TLC: Rf = 0.5 (50% EtOAc në Hex) i vizualizuar me njollë Ce-Mo1H NMR (600MHz, CDCl3) delta 1.47 (s, 9H), 2.88 (br s, IH), 3.41 (br s, 2H), 3.76 (br s, 2H).
90,1 g (1,2 mol) 2-(metilamino)etanol u tretën në 1,2 L klorur metilen, 218 g (1 mol) Boc2O iu shtuan ngadalë, ndërsa tretësira që rezulton trazohej në 0C dhe tretësira që rezulton trazohej në temperatura e dhomës për 3 orë.Përzierja e reaksionit u la në mënyrë sekuenciale me 700 mL të një solucion ujor të ngopur të klorurit të amonit dhe 300 mL ujë, u dehidratua duke përdorur sulfat natriumi anhidrik dhe më pas u përqendrua nën presion të reduktuar për të marrë 175 g (1 mol) të një përbërje vaji akromik të mbrojtur nga Grupi Boc (rendimenti: 100%).[0140] 1H NMR (600 MHz, CDCl3) delta 7.84 (br s, 2H), 7.76 (br s, 2H), 4.34 (d, J = 15.0 Hz, 2H), 3.63 (br s, 2H), 3.04 (d , J = 15,0 Hz, 3H), 1,46 (d, J = 16,2 Hz, 9H) [0141] 90 g (0,514 mol) e përbërjes së përftuar u tretën në 1,5 L tetrahidrofuran, 88,0 g (539 mol) N- Hidroksiftalimid dhe 141 g (0,539 mol) trifenilfosfinë iu shtuan, 106 ml (0,539 mol) diizopropil azodikarboksilate iu shtuan ngadalë duke trazuar tretësirën që rezulton në 0C dhe tretësira e përftuar u trazua për 3 orë ndërsa u ngrit temperatura. në temperaturën e dhomës.Pas përqendrimit të përzierjes së reaksionit nën presion të reduktuar, 600 mL izopropileter u shtuan, tretësira që rezulton u trazua në 0C për 1 orë dhe oksidi i bardhë i ngurtë i trifenilfosfinës u filtua.Lënda e ngurtë u la me 200 mL izopropileter i ftohur në 0C dhe u mblodh me filtratin e parë, dhe filtrati që rezulton u përqendrua nën presion të reduktuar për të marrë 198 g të një përzierjeje të Përbërjes XX dhe diizopropil hidrazodikarboksilate në një raport përzierjeje prej 10 deri në 15%. (rendimenti: 120%).[0142] 1H NMR (600 MHz, CDCl3) delta 7.84 (br s, 2H), 7.76 (br s, 2H), 4.34 (d, J = 15.0 Hz, 2H), 3.63 (br s, 2H), 3.04 (d , J = 15,0 Hz, 3H), 1,46 (d, J= 16,2 Hz, 9H)
 Ndërtesa 12, Nr.309, Rruga e 2-të Jugore, Zona e Zhvillimit Ekonomik, Distrikti Longquanyi, Chengdu, Sichuan, Kinë.
Ndërtesa 12, Nr.309, Rruga e 2-të Jugore, Zona e Zhvillimit Ekonomik, Distrikti Longquanyi, Chengdu, Sichuan, Kinë. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404



















.png)


